ループ押し出し

前回のブログでも少しお話しした通り、名古屋大学に着任した当時は複合材料を研究する部署にいたため、遺伝子発現制御の研究をする時間は基本的には土日しかとれませんでした。
そのうちに、朝6~7時くらいに大学に来て、論文を読むようになりました。
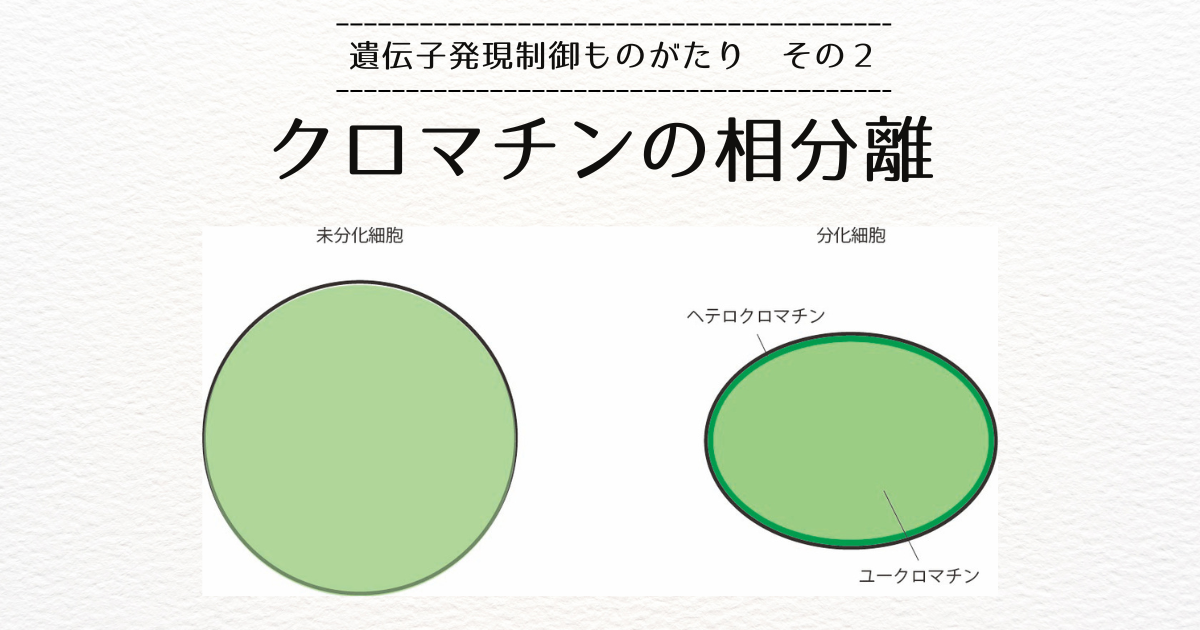
前回のブログでお話しした通り、核くらいのスケールでは、クロマチンはユークロマチン領域とヘテロクロマチン領域に分かれています。
逆に、ナノメートルの長さスケールでは、DNAはヌクレオソームを形成しています。
しかし、その間のスケール(DNAの長さでいうと1キロから1メガ塩基対くらい)でクロマチンがどのような構造を形成しているかということは長らくわかっていませんでした。
そこに一石を投じたのが2009年に発表されたHi-Cです。
Hi-Cは、染色体をセグメントに分けたとき、それぞれのセグメントがどれくらいの頻度で接触するかということを測定する技術で、Liberman-AidenらのScience論文に概略がまとめられています。
染色体は、topologically associated domain(TAD)と呼ばれるドメインに分かれていることを発見した論文がNatureに2つ同時に発表されました(Dixonらの論文とNoraらの論文)。
TADは、ドメインの内部にあるセグメントは接触頻度が高いのですが、異なるドメインのセグメントの間の接触頻度は低いという特徴を持ちます。
TADの両端で接触頻度が最大になることがしめされ、TADの正体はクロマチンのループ、または、ループの集合であることが、2014年のRaoらの論文で報告されました。
2015-2016年当時は、Hi-Cの論文が面白い事実を含んでいることを直感していましたが、分子生物学実験の論文を読むのが非常に困難で、何が書いてあるのかほとんどわからず、毎朝論文を読むのに挑戦しては打ち砕かれる毎日を送っていました。
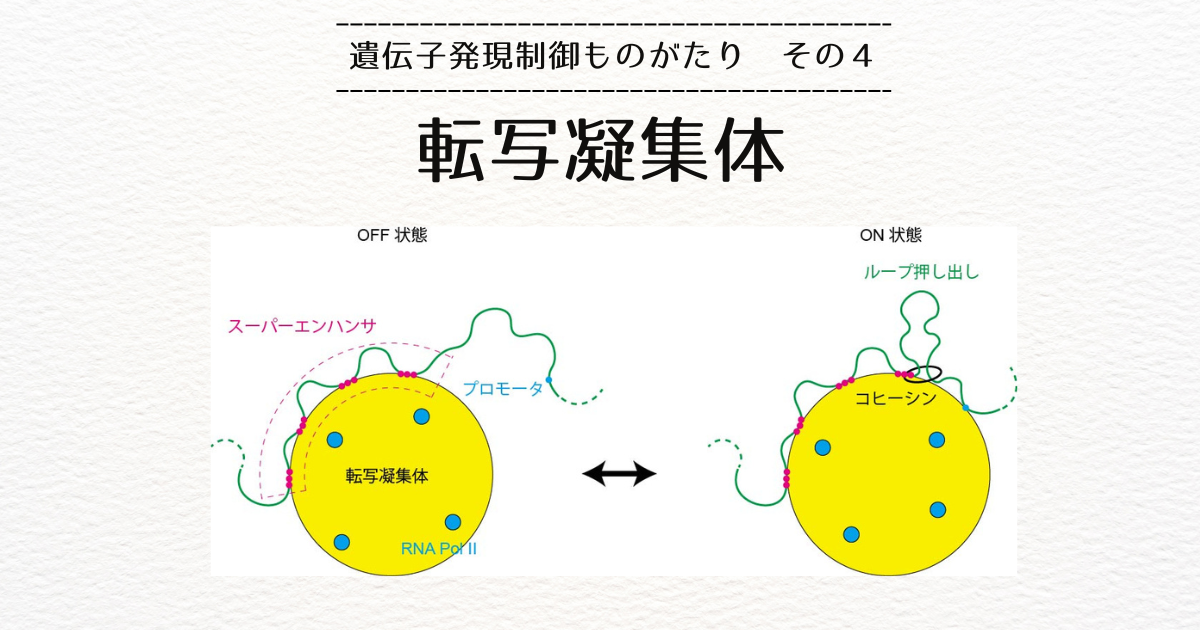
その間、前回のブログで紹介した転写によって駆動されるクロマチンの相分離の理論をHelmut Schiesselさんと作っていたわけですが、2017年初めにHelmutさんが、ループ押し出し(loop extrusion)という面白い現象があって、その研究をしてみたいという連絡が来ました。
その連絡で、これからLeonid Mirnyに会うんだということも言ってました。
コヒーシン(cohesin)というリング状のタンパク質複合体が、DNAを内包することによってループを作ります。
Leonid Mirnyさんは、コヒーシンがDNAを一方向に押し出す分子モータであると考えて、シミュレーションをしたところ、Hi-C実験で得られた接触頻度を再現することができることを示し、Cell Reportの論文で報告しました。
どちらが最初かという議論はあるようなのですが、Liberman-Aidenさんも同じ結論を得て、PNASの論文で報告しています。
Hi-Cの結果から面白いことを見つけたいと思っていましたので、やられたと思いました。
一方、Eric Greenさんのグループ、Jan-Michael Petersさんのグループ、西山朋子さんのグループが、それぞれ、DNAにロードされたコヒーシンの運動を再構成系で観察しており、コヒーシンは分子モータではないという結論を出していました。
そこで、私たちは反撃に出ることにしました。
コヒーシンが分子モータでないとしたら、どのようなメカニズムでループ押し出しが起こるのでしょうか?
コヒーシンはリング状のタンパク質複合体であり、その穴にDNAを通すことによってループを作ることは、前述のとおりです。
合成高分子の世界に、スライドリングゲルというものがあります。
スライドリングゲルは、リング状の分子をたくさん持っている高分子(ポリロタキサン)を使って、その一部のリングを二量体化することによって作られるゲルです。
その名の通り、リング状の分子は高分子をスライドすることができます。
二量体は高分子を架橋してゲル化する役割があるのに対して、単量体は高分子上を熱運動して浸透圧を発生します。
この浸透圧がスライドリングゲルの弾性の原因となっていると考えられています(真弓さんらのSoft Matter論文)。
コヒーシンは、ローダータンパク質であるNIPBL/Mau2によってDNAに搭載されます。
当時は、コヒーシン1つでループを作ることができるという考え方もあったと思いますが、コヒーシンのリングは比較的小さく、DNA一本しか通さないので、ループを作るためには二量体を作る必要があるという考え方が主流だったと思います。
私は、コヒーシンがローダーにたまたま2つ同時についた時には二量体としてDNAにロードされ、DNAループを作るのに対して、コヒーシンが1つだけしかつかなかった場合には単量体としてDNAにロードされ、浸透圧を発生すると考えました。
つまり、単量体のコヒーシンの熱運動によって発生する浸透圧をエンジンとして、二量体がループ押し出しを行うと考えたわけです。
私たちは、このループ押し出しの浸透圧機構の理論をまとめた論文をアメリカ物理学会のPhysical Review Eという雑誌に報告しました。
驚いたことに、ほぼ同時に、前のブログでも出てきたDavide Marenduzzoらのグループが、二量体のみを考えたバージョンをPhysical Review Lettersで発表しました。
そこではじめて、Leonid MirnyのグループとDavide Marenduzzoのグループが私の競争相手だということを知りました。
MirnyやMarenduzzoは自分のグループを持っていますし、おそらく、自分の興味に従って自由に研究できる環境を持っているでしょう。
一方、私はグループをもっておらず、自分の研究ができる時間は早朝と土日だけだったわけで、こんな状況でどうやって彼らに勝てばいいのだろうと、自分の置かれている状況が心底嫌になったのを覚えています。
ループ押し出しの浸透圧機構は結構自信があったのですが、本質的に同じアイデアを他の人が独立に思いつくことができるのであれば、オリジナリティーは弱いと言わざるを得ません。
そのため、私は浸透圧機構の研究をつづけることなく、代わりに、ループ押し出しが遺伝子発現に与える影響を明らかにする研究に舵をきることとなります。
しかも、2019年に、Jan-Michael Petersのグループが、cohesinのループ押出しを一分子計測で観察することに成功し、Scienceにその結果を報告しました。
Cohesinがループ押し出し運動をするためには、ローダーであるNIPBL/Mau2が必須という結論でした。
結局、浸透圧機構も机上の空論に終わったこととなります。
しかし、この浸透圧機構の論文を通したことによって、西山朋子さん、平野達也さん、白髭克彦さんなどのコヒーシンをはじめとしたSMCタンパク質の研究者と出会うことができました。
また、この論文を契機に科研費にも採択されるようになり、また、さきがけのゲノム合成領域にも採択され、私の研究は質的に変わっていくこととなります。
前回のブログと同じ結論ですが、ちゃんと論文を出すことは、人と出会い、成長し、よりよい研究をするのに重要なのだと思います。
アインシュタインは、”A person who never made a mistake never tried anything new.”(間違えを犯したことのない人間は、新しいことに挑戦しない人間だ)という格言を残しています。
名古屋大学は、この格言を心の支えとしていた時代でした。