DNAブラシの転写
遺伝子発現制御と聞いて、これを物理の問題だと考える人はまだ少ないと思います。
私がこの研究を始めたときにはもっと少なかったです。
というのは、遺伝子発現はもっぱら生命科学で研究されてきたからです。
遺伝子発現制御とは何かということは、軽く以前の記事で触れました。
要約すると、生命の遺伝情報(設計図)はDNAの塩基配列という形で蓄えられています。
我々のような多くの細胞から個体が形成されている多細胞生物では、すべての細胞がおなじ塩基配列を持つDNAを持っています。
筋肉の細胞と脳の細胞が異なる働きをしているように、設計図は同じなのに、異なる性質を持つ細胞が形成されるのはなぜかというと、それぞれの遺伝子が使われる(発現する)頻度が細胞の種類ごとに異なるからです。
遺伝子の発現は、同じ配列(正確には相補的な配列)を持つRNAを合成する転写というプロセスから始まり、翻訳というプロセスにて、RNAの塩基配列に対応するタンパク質が作られるという形で進みます。
細胞の機能はこのように合成されたタンパク質によって発現しますが、それぞれの遺伝子の発現頻度が異なる細胞は性質も異なってくることが様々な種類の細胞ができるメカニズムです。
それでは、細胞はどのように遺伝子の発現頻度を制御しているのでしょうか?という問いに、あえて物理で答えるのが私の研究です。
この研究に取り組むきっかけとなったのは、イスラエルのヴァイツマン研究所での研究経験です。
ヴァイツマン研究所では、所内の実験の研究者ならばだれとでもいいから、共同研究をしてなにか成果を上げなさいという、比較的自由度の高いミッションが与えられていました。
その前にいたドイツのMax Planck研究所でも同様なミッションだったので、海外の国立研究所で研究員(ポスドク)をすると、わりと自由度が高いのだと思います。
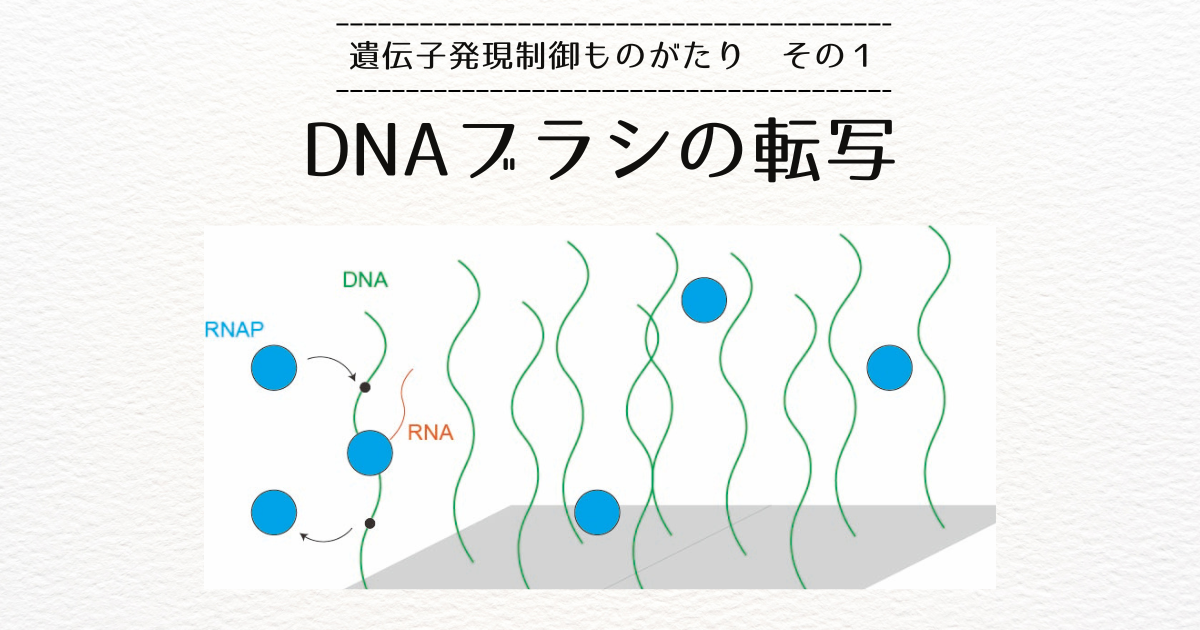
この研究所には、Roy Bar-Zivさんという先生がいらっしゃいまして、たくさんのDNAの方端を表面につけてつくられるDNAブラシというものを作って、転写をさせるという実験をされていました。
ナイーブには、表面に結合するDNAの数を大きくすると、それに比例してRNAが合成される速度もそれに比例して大きくなると考えられるのですが、実はそうはならず、あるところで飽和するという実験結果が得られていました。
また、転写される遺伝子の開始側の端を表面につけた場合と終端側の端をつけた場合で、RNAの合成速度が2倍程度変わるという結果も得られていました。
この実験結果は、PNASという雑誌に掲載されています。
私は、化学反応速度論を使って転写を扱い、高分子物理を使ってDNAブラシを扱うことによって、この実験の原因を理論的に調べてみることにしました。
化学反応速度論を使って転写をどのように扱うかということがこの理論の困難だったのですが、定常状態では、転写開始位置でRNA合成酵素(RNAポリメラーゼ)が溶液からDNAに一定速度でつき(シンク)、転写終端位置ではRNAポリメラーゼがDNAから溶液に同じ速度で解離していく(ソース)ことに注目しました。
このように転写を見ると、RNAポリメラーゼの反応には、「誘電分極」という、コンデンサやメモリで電気がたまるのと本質的に同じ原理がはたらいていることに気づきました。
この理論を使って、DNAの数を大きくするとブラシ内のDNA密度が大きくなり、ブラシ内のRNAポリメラーゼの数が減ることがRNA合成の飽和の原因であること、また、転写によって転写開始位置から終端位置にRNAポリメラーゼが移動することにより、ブラシ内でRNAポリメラーゼの濃度勾配ができることによってBar-Ziv先生の実験結果を説明することができることがわかりました。
この理論をまとめた論文は、英国王立化学会(Royal Society of Chemistry)のSoft Matterという雑誌に掲載されました。
この理論を見て、当時の私のボスのSamuel Safran先生に、お前の理論には化学反応が入っているので嫌いだと言われてしまいました。
今考えると、ボスにお前の理論は嫌いだと言われたので、へこむのが普通かもしれませんが、当時の私は、物理の人が化学反応が苦手なら、ソフトマター物理と化学反応を組み合わせる課題は私がやろうと思いました。
DNAブラシは、実際の細胞の状況と非常に異なると思われたかもしれません。
しかし、その理論を作ることで得た、遺伝子発現の頻度は遺伝子の周りの構造によって制御される、遺伝子発現自体が系の構造に影響を与える、という知見は、実際の細胞での遺伝子発現の研究をするうえで重要な視点になると考えました。
その視点で、分子生物学者が明らかにしてきた遺伝子発現制御のメカニズムを見てみると、細胞内の様々な構造が遺伝子発現を制御する例が豊富にあることに気づきます。
ソフトマター物理と化学反応速度論を組み合わせるというアプローチは、実際の細胞の遺伝子発現制御のメカニズムを調べる上でも有用ということです。
幸いにも、ソフトマターの自己組織化(放っておいても勝手に分子が集まって構造が作られる現象)をヴァイツマン研究所で、その後、非平衡ダイナミクス(運動をかっこよく言うとこうなる)も習得することができましたので、遺伝子発現制御を理論物理のアプローチで解き明かすための基礎スキルも身に着けることができました。
名古屋大で助教に採用されたとき、比較的自由に研究させていただける環境だったので、遺伝子発現制御の問題にチャレンジしてみたというわけです。