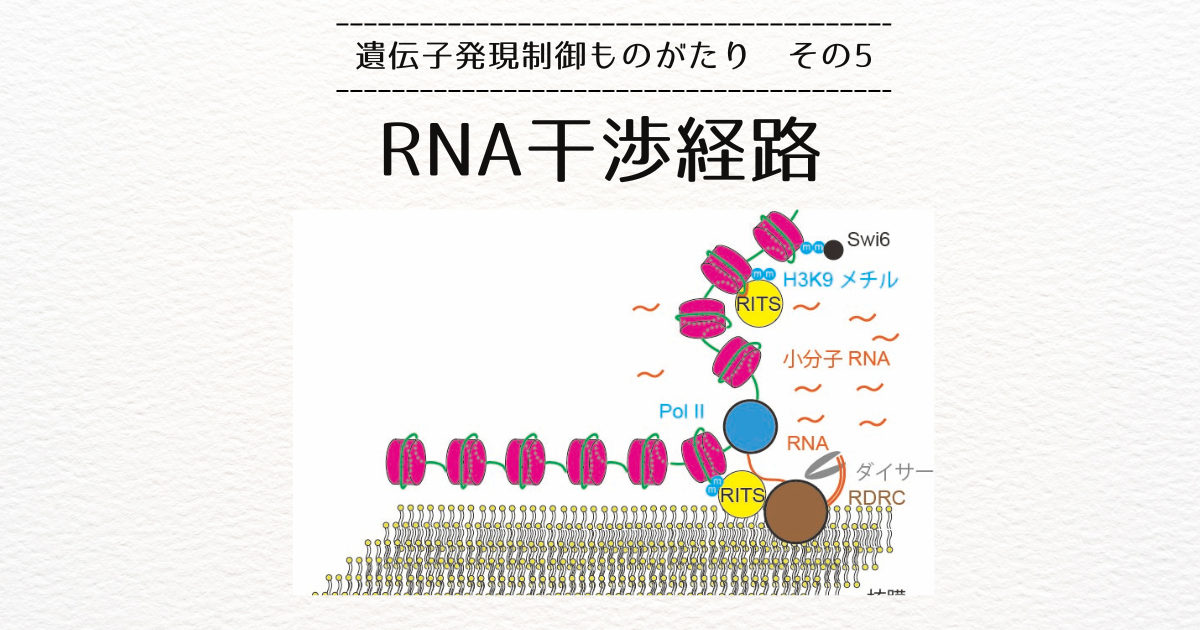
クロマチンの相分離
ヒトやマウス、植物などの細胞や酵母などのように、細胞内に核を持つ生物を真核生物と言います。
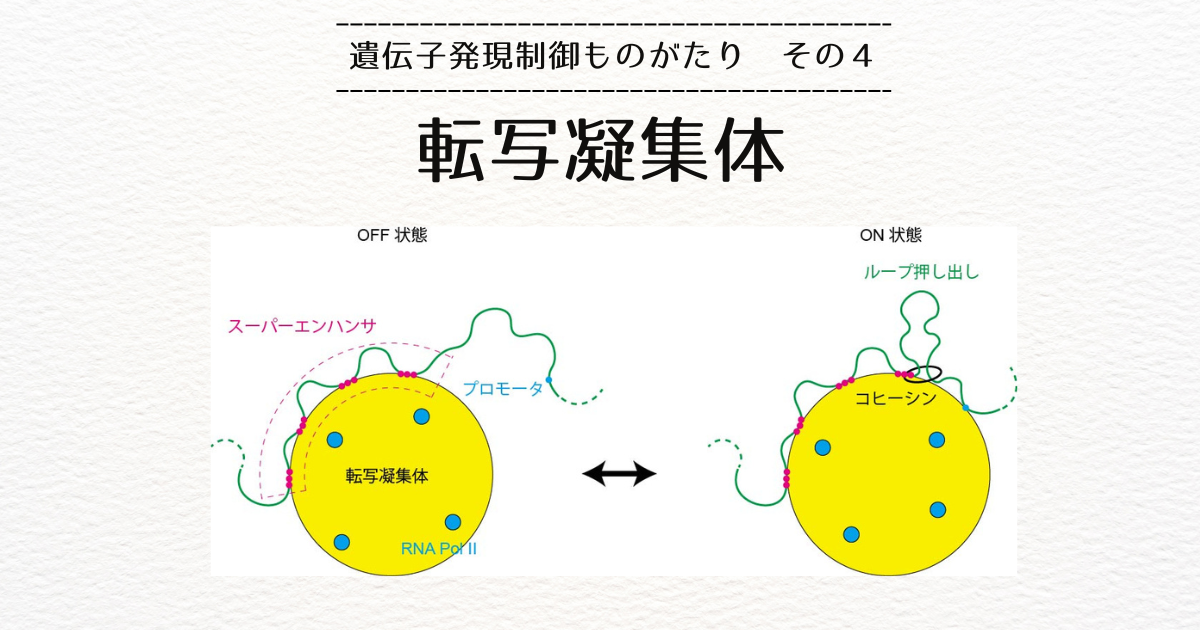
ヒトのDNAは全長2メートルということを聞いたことがあるかもしれませんが、それほどの長さのDNAを核のようなマイクロメートルの空間に閉じ込めるために、ヒストンというタンパク質と一緒にクロマチンという構造を形成しています。
クロマチンはDNAから形成されているので、ひも状の物質なのですが、その繰り返し単位は、ヒストン8つにDNAが巻き付いたような構造(ヌクレオソーム)となっています。
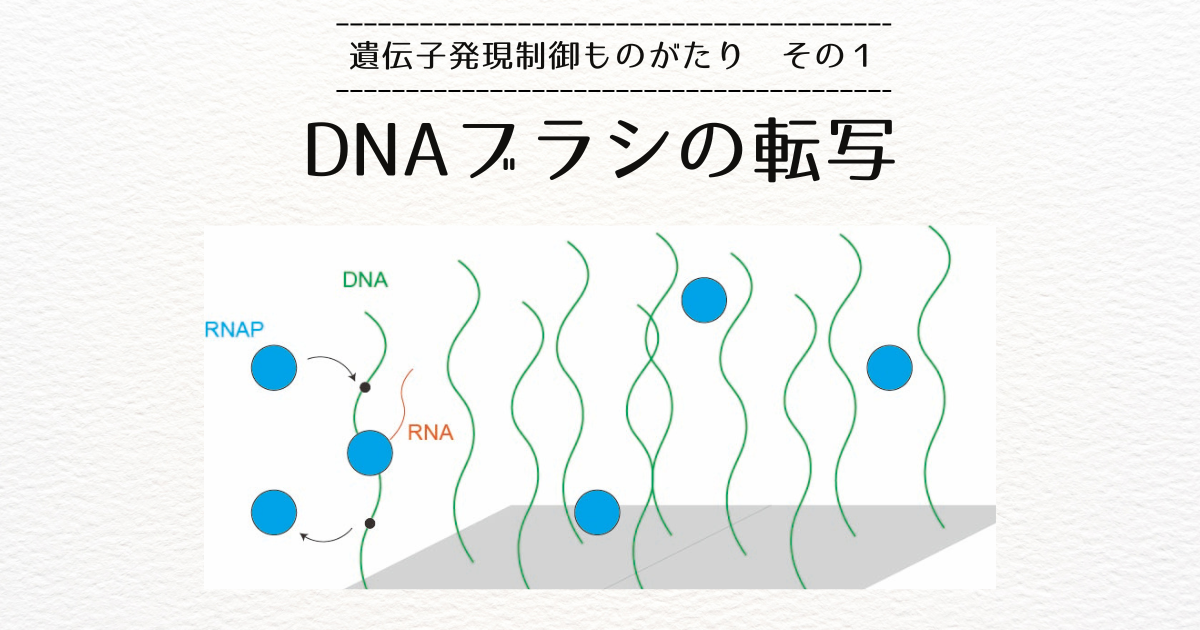
前回お話ししたDNAブラシでは、ヌクレオソームを形成していない裸のDNAを扱っていました。
そこで、名古屋大学の助教に着任してからは、DNAブラシの理論をクロマチンに拡張することから研究を始めました。
すでにヌクレオソームとクロマチンの構造は物理の問題になっていて、その理論の第一人者は、2015年当時オランダのライデン大学にいた(2026年2月現在ドレスデン工科大にいる)Helmut Schiesselさんという方でした。
クロマチンに関してはど素人でしたので、Schiesselさんと共同研究する形で研究をスタートしいました。
Schiesselさんに、DNAブラシの転写の理論をクロマチンに拡張する構想をお話ししたとき、転写の間にRNAポリメラーゼがヌクレオソームと衝突すると、ヒストンがDNAから取れてしまうことを試験管実験で示した論文を紹介していただきました。
ここで、試験管実験とは、生きた細胞内ではなく、DNAとRNAポリメラーゼなどの転写に必要なタンパク質を精製し、精製タンパク質の水溶液中で行った再構成実験のことです。
この論文を読んだとき、この衝突を考えると、ヌクレオソーム間の相互作用と転写を考慮に入れることで、クロマチンの相分離を予言することができることに気づきました。
この相分離では、転写が盛んな部分ではDNAが膨潤していて、転写が抑制されている部分ではDNAはクロマチンを形成して収縮しています。
皆様は幹細胞とかiPS細胞のことを聞いたことがあるかもしれません。
このような細胞は、いろいろな種類の細胞に変わる(分化する)ことができる細胞です。
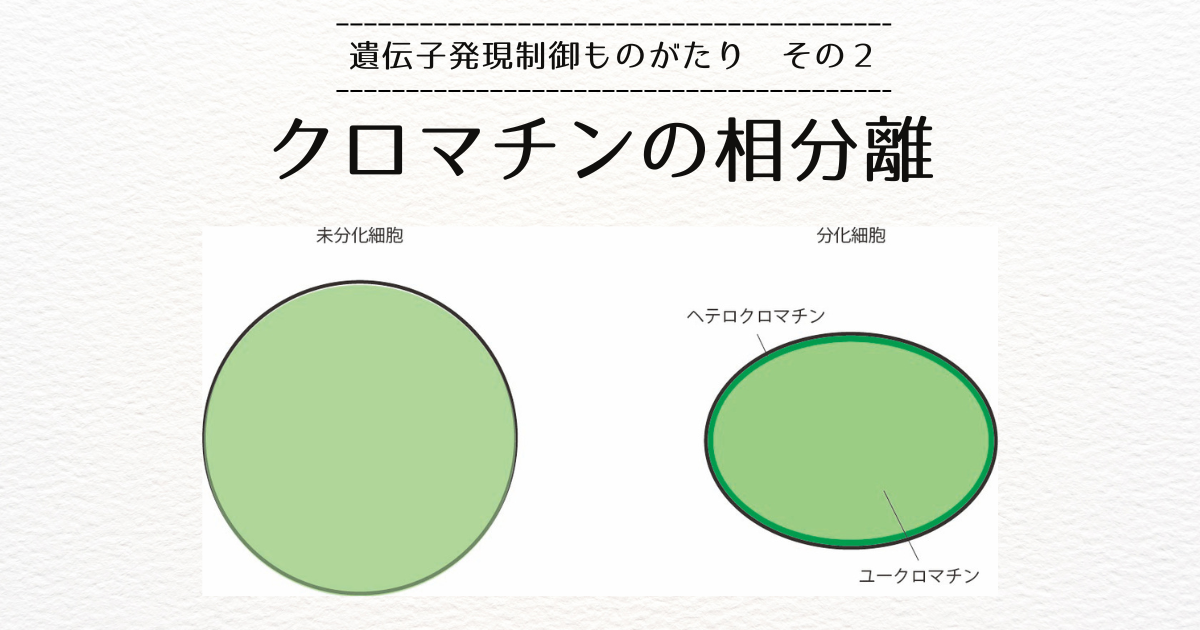
分化細胞のクロマチンは、ユークロマチンと呼ばれる転写が活性で比較的密度が低い領域とヘテロクロマチンと呼ばれる比較的密度が濃い領域に分かれています。
このことは転写によるクロマチンの相分離の理論の予言と整合しています。
実は、ユークロマチンとヘテロクロマチンが相分離によって形成されることを理論的に示した先駆者はPeter CookとDavide Marenduzzoで、2009年にJournal of Cell Biologyという雑誌に報告されています。
多くの分化細胞では、ヘテロクロマチンは核膜付近に局在化していて、ユークロマチンは核の中央付近に局在化していることが電子顕微鏡などで観察されています(たとえば、Susan Gasserさんのレビュー論文)。
しかし、夜行性の動物の目の細胞では、ヘテロクロマチンが中心に局在化していて、ユークロマチンが核膜付近に局在化することをIrina SoloveiさんらがCellの論文で報告しています。
また、核膜にあるラミンBレセプタとラミンA/Cをなくすと、通常の分化細胞(夜行性動物の目の細胞以外)でもユークロマチンが核膜側、ヘテロクロマチンが中央側に配置されることを後続論文で報告しています。
CookとMarenduzzoの論文は、ユークロマチンとヘテロクロマチンの配置を理解するためのもので、クロマチンはすでにユークロマチンと類似した性質を持つ部分とクロマチンと類似した性質を持つ部分に分かれている前提で議論が始まります。
一方、我々の理論は、一様なクロマチンがどのようにユークロマチン的な部分とヘテロクロマチン的な部分に分かれるかということ(対称性の破れ)が議論の中心となっています。
分化する前の細胞(未分化細胞)では、クロマチンはほぼ一様な構造を形成しています。
未分化細胞は比較的球形で体積が大きいのですが、分化するにつれて扁平となり体積も小さくなることが、遺伝研の木村暁さんのScientific Review論文で報告されています。
DNAの量は一定ですので、分化するにつれてDNAの濃度が高くなるということです。
我々の理論で、相分離を駆動する要素は圧力を加えることによるクロマチン濃度の増加ですので、木村暁さんの実験結果と整合しています。
転写によるクロマチンの相分離の理論の論文は、アメリカ化学会のLangmuirという雑誌に掲載されました。
またどこかでお話しするかもしれませんが、名古屋大学に着任した2015年は、複合材料の研究をする部署に配属されていたため、クロマチンの相分離の研究は土日で行っていました。
それでも、このプロジェクトを1年間でやり遂げて、2016年の3月までに論文を出すことができました。
その後、相分離によって形成される構造の詳細に関する理論をRoyal Society of ChemistryのSoft Matterという雑誌に、相分離のために核が負のポアソン比を持つことを予言する理論をひヨーロッパの物理学会誌であるEurophysics Letters誌に報告しました。
我々の理論は、RNAポリメラーゼがヌクレオソームと衝突すると、ヒストンがDNAから取れてしまうことを前提としています。
しかし、現在では、東大の胡桃坂さんが、FACTというタンパク質(シャペロン)によって、ヒストンはDNAから完全にはがれるわけではなく、後方に新しいヌクレオソームを作ることをクライオ電子顕微鏡で示し、その論文をScienceに報告しています。
理論を作るのに参考にした試験管実験では、FACTが足りてなかったのです。。。
試験管実験は系が比較的単純なのが長所ですが、必要な因子が足りていない場合があるところが怖いですね。
その意味で、我々が考案した、転写によって駆動されるクロマチン相分離の理論は、机上の空論だったのだと思います。
しかし、この研究を行い、論文を書いたことは、Helmut Schiesselさんだけでなく、新学術木村領域(クロマチン潜在能)に参加し、日本の様々な分子生物学者と出会い、交流し、共同研究を行っていくきっかけになりました。
一般的には、自分が成長し続けている限り、現在行っている研究よりも、未来に行う研究の方が良いものになる可能性は高いと思います。
自信がなくても、ちゃんと論文にすることは、人と出会い、成長し、未来の研究をよくするきっかけとなるので、重要なことなのだと思います。