転写凝集体
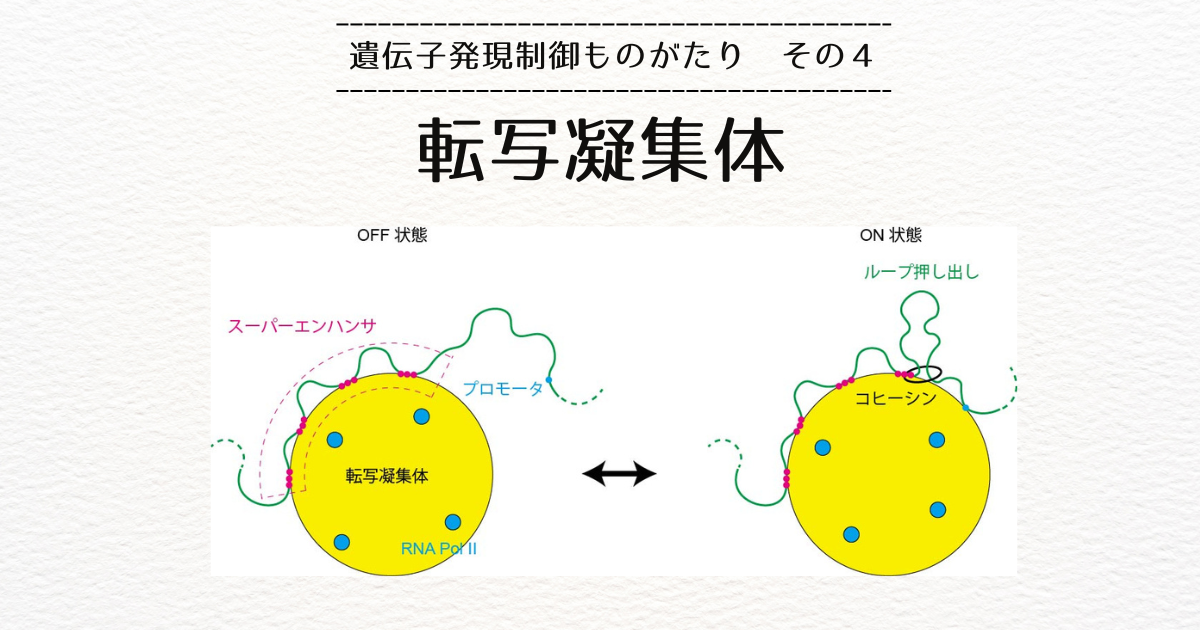
ループ押し出しと遺伝子発現制御
前回のブログで、10ー1000キロ塩基対の長さでは、DNAはループを形成していることと、コヒーシンというリング状のタンパク質がDNAを内包することによってループができることをお話ししました。
また、コヒーシンは分子モータであり、DNAを一方向に押し出す運動(ループ押し出し)を行うと仮定すると、ドメイン内部のセグメント間の接触頻度は高いのに、異なるドメインに属するセグメント間の接触頻度が低いというtopologically associated domain(TAD)の性質を説明することができるというMirnyの理論をご紹介しました。
それでは、遺伝子発現制御の観点からいうと、ループ押し出しは重要なのでしょうか?
それは、エンハンサというDNA制御配列と関係があります。
エンハンサは、転写活性化因子(単に転写因子とも呼ばれる)が結合するDNA部位です。
エンハンサに結合した転写因子には、さらに、全体の構造のハブとなるコアメディエータ複合体と、RNAを合成するのに必要なRNA合成酵素(RNA Pol II)が結合します。
遺伝子の転写開始位置にもプロモータと呼ばれる制御配列があります。
DNAがループを作って、プロモータとエンハンサが相互作用すると、必要な因子がプロモータに渡され、転写が活性化するというのが当時の常識でした。
TAD内の接触頻度が高く、TAD間の接触頻度が低いということは、エンハンサはドメイン内部の遺伝子を選択的に活性化することを示唆しています。
それでは、コヒーシンを壊して、クロマチンループをなくしてしまうと、転写量はどのように変化するでしょうか。
そのような実験が、そのような実験が、2017年にLieberman-AidenらのグループとMirnyらのグループから、それぞれCellとNatureという雑誌に報告されています。
コヒーシンを壊すと(正確には、コヒーシンのサブユニットを壊すかローダータンパク質を壊すことによって、コヒーシンがDNAにロードできないようにすると)、転写量が増加する遺伝子もあれば、減少している遺伝子もあるため、変化量も比較的小さい(2倍程度)ため、効果がよくわからないという結果でした。
ただし、Lieberman-Aidenらの論文には、スーパーエンハンサと呼ばれる特別なエンハンサの標的遺伝子に対しては、コヒーシンを壊すと有意に転写量が減少することを報告しています。
エンハンサがある程度密に詰まっているゲノム領域をスーパーエンハンサといいます。
多数のエンハンサがつながっているものと思っていただければいいと思います。
スーパーエンハンサは、Richard Youngが2013年に打ち出した概念で、たとえば、iPS細胞や幹細胞の状態を作るのに重要な役割を果たすOCT4, SOX2, NANOGなどの遺伝子は、スーパーエンハンサによって活性化されています(YoungらのCell論文)。
Lieberman-Aidenらの論文には、スーパーエンハンサには、コヒーシンのローダであるNIPBL/Mau2が多く結合しており、コヒーシンのローディングサイトとしての役割も果たしていることも報告されています。
転写凝集体
スーパーエンハンサに関しては、全く別のタイプの実験によって面白いことが報告されています。
先ほどご紹介した、転写活性化因子、コアメディエータ、RNA Pol IIは、相分離を起こして凝集体を形成するということがRichard YoungグループとClifford Brangwynneのグループによって、それぞれ、ScienceとCellという雑誌に報告されました。
このような凝集体を転写凝集体といいます。
Youngらの論文では、スーパーエンハンサが転写凝集体の表面についていることが示唆されています。
スーパーエンハンサの標的遺伝子はどこにあるかというと、転写凝集体にあるものもあれば、そうでないものがあるということもIbrahim CisseらのグループがScienceという雑誌に報告しています。
実験事実のまとめ
長くなってしまったので、ここで実験事実を整理しましょうか。
①コヒーシンを壊してTADをなくしてしまうと、スーパーエンハンサの標的遺伝子の転写量が減少する。
②コヒーシンは、スーパーエンハンサからDNAにロードされる。
③スーパーエンハンサは、転写凝集体の表面についている。
④スーパーエンハンサの標的遺伝子は、転写凝集体についているものもあれば、ついていないものもある。
界面のDNAのループ押し出し
ループ押し出しはどのようにスーパーエンハンサの標的遺伝子の転写量を制御しているのでしょうか?
スーパーエンハンサは転写凝集体の表面につなぎ留められていますので、表面のDNAの運動がその謎を解くカギになると考えられます。
DNAは高分子の一種ですが、高分子の運動の基本的なモデルとして、ラウス(Rouse)モデルというものがあります。
私は、コヒーシンによるループ押し出し運動を考慮に入れて、ラウスモデルを拡張することから研究を始めました。
このプロジェクトには、ドレスデン工科大のHelmut Schiesselさんに加えて、青山学院大学の坂上貴洋さんにも加わっていただきました。
坂上さんは高分子のスケーリング理論のエキスパートで、私も研究のスタートでは、スケーリング理論を使ってこの問題を解くことを考えていました。
しかし、ループ押し出しを考慮に入れるのが難しく、最初は全然うまくいきませんでした。
そのうち、どのようにDNAが運動するのかを見てみたくなって、2018年の11月から2019年の1月だったと思うのですが、プログラムを書いてシミュレーションをしてみました。
ちょうど、2018年にさきがけ「ゲノム合成」に採択していただき、2019年初頭に領域会議が控えていたために、何とか結果を出そうと思って頑張っていたのを覚えています。
それまで年末年始は実家で過ごしていたのですが、2019年は研究室ですごしていました。。。
シミュレーションをしているうちに、溶液中で自由拡散しているDNAと、(たとえば、スーパーエンハンサによって)界面に束縛されているDNAでは、コヒーシンがループ押し出しをした時のDNAの運動が非常に異なることがわかってきます。
高分子は同じユニットがつながったものですが、あるユニットに力を加えて動かすと、他のユニットがそれに反応するまでに時間がかかります。
高分子全体が反応する時間を緩和時間と呼ぶことが多いのですが、今はスーパーエンハンサと遺伝子のプロモータの間のDNA領域のみが重要なので、その領域が反応する時間を緩和時間ということにしましょう。
そのDNA領域の長さが長くなると、緩和時間は長くなります。
溶液中で自由拡散しているDNAは両端が自由ですので、ループ押し出しによって加わる力がすぐに緩和してしまいます。
一方、界面に束縛されているDNAは、片方の端(スーパーエンハンサ)が固定されていますが、コヒーシンは固定端にロードされてループ押し出しを始めるので(前述の実験事実②)、もう片方の自由な端は、緩和時間後に反応するのです。
シミュレーションをする間に、ループ押し出しによるDNAの運動を解析的に(ノートと鉛筆で)解くことができる方法を思いついてしまい、結局その方法でDNAの運動の基本法則を導くこととなりました。
この理論をまとめた論文は、Europhysics Lettersというヨーロッパの物理学会誌に掲載されました。
最初にとん挫したスケーリング理論ですが、最近、ループ押し出しによるDNAの運動と似た系を解くことができたので、今だったらできるかなと思います。
スケーリング理論は、今のボスであるMichael Rubinstein先生と一緒に研究することでできるようになったので、Rubinstein先生に感謝です。
転写凝集体による遺伝子発現制御
転写凝集体表面につなぎ留められているDNAの運動を調べるための理論ができましたので、これを使って、ループ押し出しがどのように遺伝子発現を制御するかということを明らかにする研究に移りました。
2021年の初頭にさいがけの領域会議が控えていたため、この理論も2020年の年末から2021年の年始にかけて作ったのを覚えています。
コロナ渦の間でしたので、研究室ではなく、自宅での研究になりました。
転写凝集体の中には、RNAポリメラーゼIIなどの転写に必要な因子が含まれていますので、遺伝子のプロモータがどれくらいの頻度で転写凝集体にアクセスできるかということを、ループ押し出しがある場合とない場合について計算してみました。
その結果、ループ押し出しがない場合(たとえば、コヒーシンを壊した場合)には、スーパーエンハンサープロモータ間のDNAは単純に熱運動を行います。
ループ押し出しがある場合には、加えられる力によって、プロモータが転写凝集体の方向に引き込まれるため、凝集体内部のRNAポリメラーゼIIにアクセスする頻度が高くなることがわかりました。
コヒーシンが取れてしまうと、プロモータがもとの位置に戻ってしまいますが、そのために必要な時間が、前述の緩和時間です。
緩和時間の前に新しいコヒーシンがロードされ、ループ押し出しを始めると、元に戻る前にまた凝集体の方向に引き込まれます。
スーパーエンハンサープロモータ間のDNAの長さが長いほど、緩和時間も長くなります。
その結果、スーパーエンハンサープロモータ間のDNA長を長くしていくと、最初は転写レートが小さくなるのに、ある長さで最小値をとった後、今度は転写レートが大きくなることがわかりました。
これは、正直、予想外の結果でした。
実験とは異なり、理論で予想外の結果が出ることは非常に稀ですので、とてもうれしかったのを覚えています。
この理論をまとめた論文は、Oxford出版社のNucleic Acids Researchという雑誌に掲載されています。
このあたりから「世界で初めて」の理論を作ることが多くなってきます。
一方、複数の実験論文を読んで、それを説明するための一般原理を考えるというスタイルは、この研究の後、少なくなっていきます。
転写凝集体とスーパーエンハンサによる転写制御は、現在でも精力的に研究されていまして、その全貌はまだ明らかになっていませんし、我々の理論も実験的な検証はまだです。
どのような結末になるか、楽しみです。