RNA干渉経路
分裂酵母では繰り返し配列の転写が不活性化される
分裂酵母のヘテロクロマチン形成には転写が必要
真核生物のDNA(染色体)の中央の部分はセントロメアと呼ばれる領域で、同じ塩基配列が繰り返されている配列(繰り返し配列)となっています。
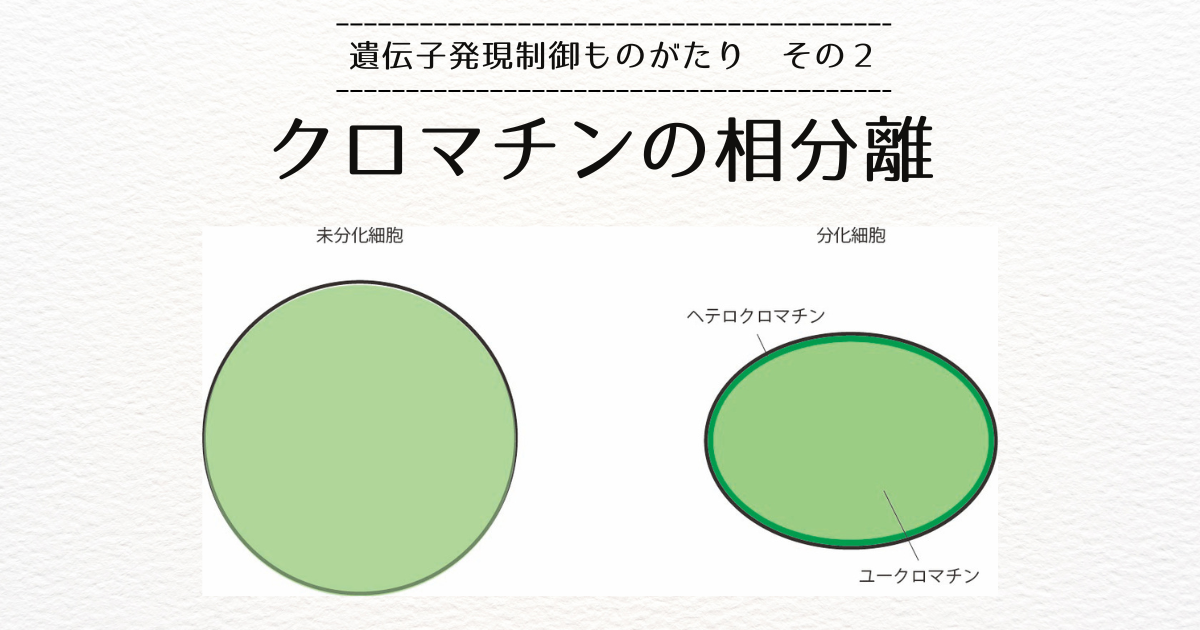
セントロメア領域は、一般的に転写が不活性なヘテロクロマチン領域となっています。
前のブログでも紹介しましたが、真核生物のDNAは裸ではなく、ヒストンの複合体であるクロマチンを形成します。
その繰り返し単位がヌクレオソームでしたね。
ヌクレオソームは、ヒストン8つにDNAが巻き付いた構造をしていますが、その内訳は、H2A, H2B, H3, H4という異なるものが2つずつとなっています。
セントロメア領域のクロマチンは、ヒストンH3の9番目のリジン(アミノ酸)がメチル化しているという特徴を持っています。
専門的には、H3K9me(ヒストンH3の9番目のリジンKがメチル化)と書きます。
もう少し詳しい話をすると、分裂酵母ではメチルが2つ付いたH3K9me2が、高等生物ではメチルが3つついたH3K9me3がよく出てきますが、ここではざっくりH3K9meと書いておきます。
分裂酵母は、真核生物の研究でよく研究されている生物(モデル生物)の中でも最も原始的な生物の一つで、3本の染色体を持ちます。
分裂酵母の染色体のセントロメア領域がヘテロクロマチン化されるために必要なものを網羅的に探してみると、なんと、転写のメインプレイヤーであるRNAポリメラーゼIIがその原因分子として見つかりました。
ヘテロクロマチン領域では転写が不活性といえども、頻度が低いだけでゼロではありません。
逆説的ですが、セントロメア領域の転写が不活性化するためには、その頻度の低い転写が必要であるということです。
もう退官されましたが、北大にいらっしゃった村上洋太先生からこの話を聞いた時、とても惹かれたのを今でも覚えています。
それでは、どのようなメカニズムで転写が転写を不活性化しているのでしょうか。
RNA干渉経路
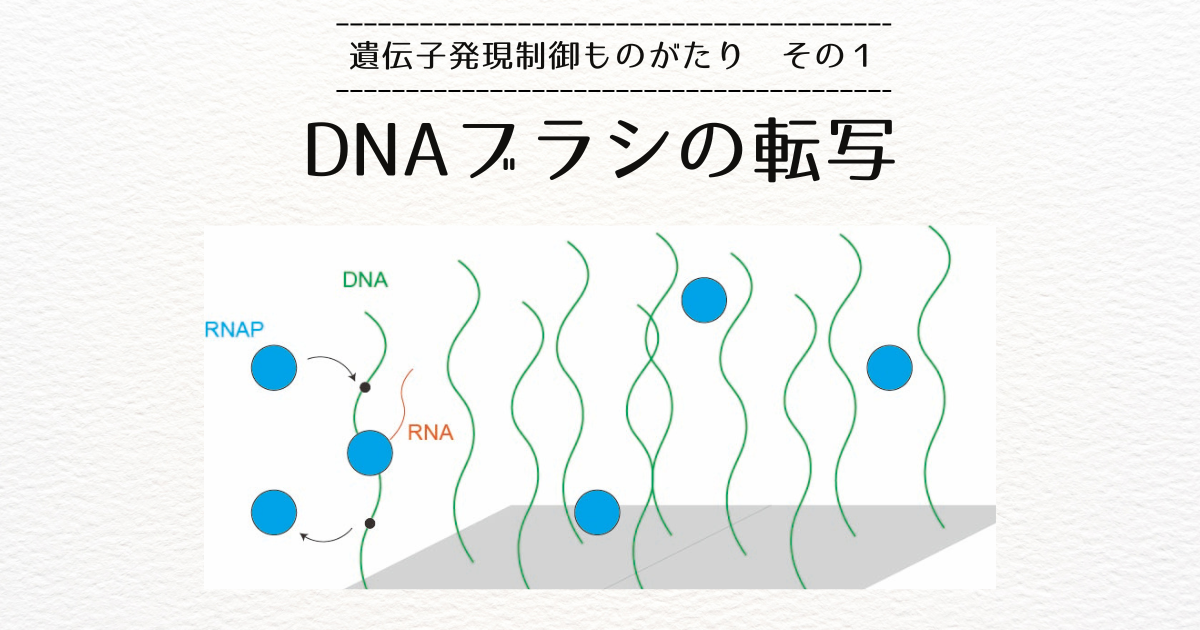
セントロメア領域がRNAポリメラーゼII(Pol II)によって転写されると、当然相補的なRNAが生成されます。
合成途中のRNA(新生RNA)は、Pol IIにつながっています。
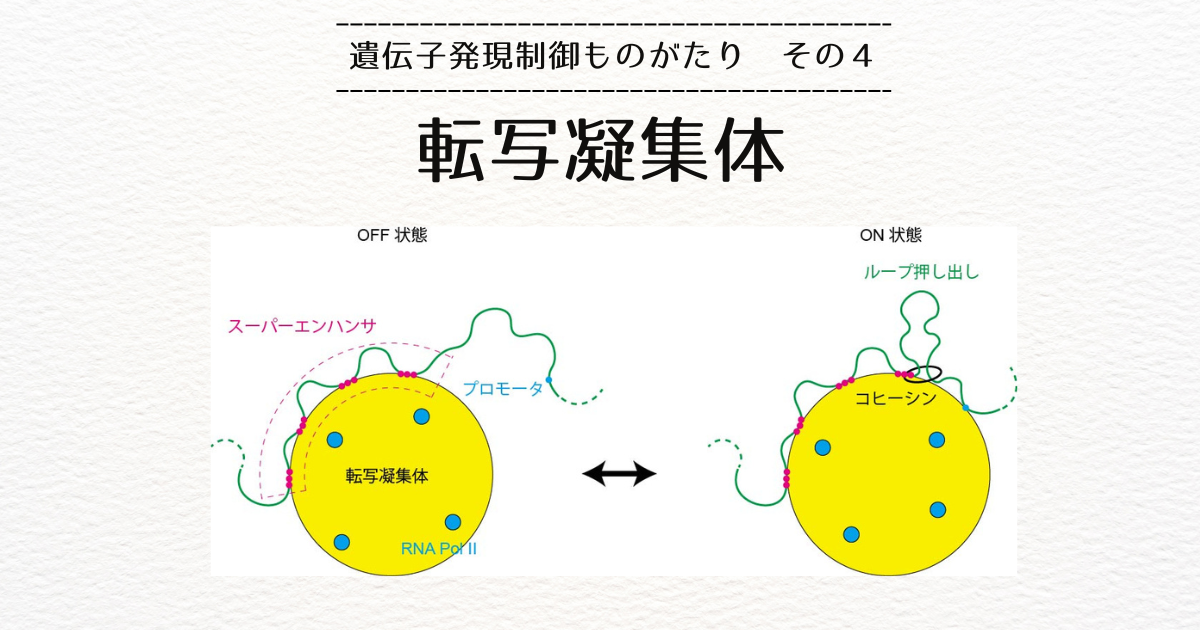
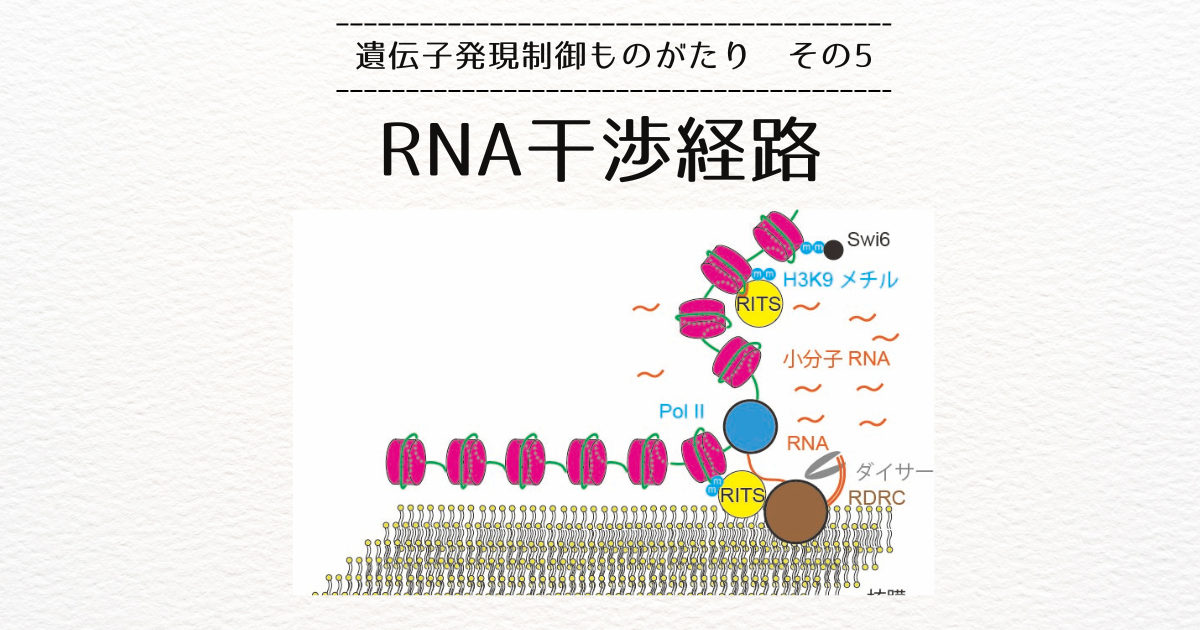
セントロメア領域のヘテロクロマチン化に中心的な役割を果たすのがRITS複合体です。
RITSはアルゴノートと呼ばれるタンパク質を含む複合体で、アルゴノートはRNAの断片(小分子RNA)を保持することができます。
RITS複合体は、メチル化酵素であるCrl4を含んでいるので、保持している小分子RNAと相補的な配列を持つ新生RNAに結合し、その場のヌクレオソームをメチル化(H3K9me)します。
一方、メチル化(H3K9me)されたヌクレオソームには、小分子RNAなしですがRITSが新生RNAをはさみこむように結合することができます。
RITS複合体は、RDRC(RNA依存的RNAポリメラーゼ)とダイサーに結合する性質を持っています。
RDRCによって挟み込んだ新生RNAを二重らせん化し、ダイサーによって二重らせんとなったRNAが断片化され、小分子RNAが生成されます。
つまり、RITS複合体はヌクレオソームのメチル化と小分子RNAの生成に必要な機能を持つタンパク質を集めるハブであり、転写によって生成される新生RNAがRITS複合体をしかるべき場所に留めておくのに必要なわけです。
リピート配列はヘテロクロマチン化される
セントロメア領域が不活性化されているのは、そこでの転写頻度が低いからだと考えられます。
そこで、当時北大にいらっしゃった浅沼高寛さんと村上洋太先生は、セントロメア領域の転写頻度を増加する実験を行いました[1]。
その結果、なんと、転写の増加に伴って、ヘテロクロマチンの特徴であるヌクレオソームのメチル化の度合いや小分子RNAの量が増加したのです。
ここで、タンパク質をコードしている活性な遺伝子ではなぜメチル化や小分子RNA生成が起こらないのに、セントロメアでは起こるのだろうという疑問が生じます。
高等生物のセントロメアが繰り返し配列となっていることをこのブログの最初にご紹介させていただいたと思います。
浅沼さんと村上先生は、活性な遺伝子を複数つなげた配列を作り、それを改造前では活性化しているユークロマチン領域に埋め込み(ノックインし)ました。
その結果、なんと、繰り返された遺伝子が不活性化されたのです!
つまり、転写の不活性化の鍵は繰り返し配列にあったのです。
繰り返し配列では同じ配列がつながっていることが分裂酵母のヘテロクロマチン形成の原因
繰り返し配列と高分子物理学
セントロメア領域の転写が定常的に不活性化されているためは、定常的に小分子RNAが生成されていなくてはなりません。
ということは、セントロメア領域は定常的に転写され、RDRCによって二重らせん化された新生RNAが定常的にダイサーに断片化されている必要があります。
私は、孤立した配列では定常的にRDRC/ダイサーと結合するのが難しく、繰り返し配列では容易いという点が、高分子の表面吸着の問題と似ていると直感的に思いました。
高分子の表面吸着の問題では、その名の通り、高分子を形成するユニットがどのように表面に吸着するかということを議論します。
その肝は、例えば、高分子の中の1つのユニットが表目に吸着していると、他のユニットは吸着しているユニットとつながっているために、表面近くにあります。
そのため、高分子を構成しているユニットは表面近くにあり、吸着しやすくなります。
つまり、同質のユニットがつながっていることが、ユニットの吸着にポジティブに働くということです。
そのことを村上先生と浅沼さんにご報告したとき、実はRDRCとダイサーが核膜に結合していることを示唆する実験があることを教えてもらいました[2,3]。
孤立している短い遺伝子では、例え転写が起きて、その生成RNAがRDRC/ダイサーに結合して断片化されている状態であっても、転写が終わると遺伝子はRDRC/ダイサーから解離してしまいます。
一方、繰り返し配列では、同じ配列を持つ遺伝子がつながっているので、その中の一つの遺伝子が転写されていて、RDRC/ダイサーと結合して小分子RNAを精製している状態であれば、つながっている他の遺伝子も核膜の近くにあるため、転写が起きればRDRC/ダイサーと結合しやすい状態にあるわけです[4]。
このアイデアは、論文が出た2023年時点では自己ベストだったと思います。
直観力をフルに利用する研究は本当に楽しい。
浅沼さんと村上先生と会うことがなければ、この理論を作ることはできなかったでしょう。
お二人には本当に感謝しています。
この理論は正真正銘「世界で初めて」だと思っています。
この研究で学んだこと
RNA干渉経路でヘテロクロマチンができるのは、分裂酵母に特有な現象であって、高等生物では他のメカニズムでヘテロクロマチンが形成されると考えられています。
物理学は自然の一般法則を究める学問ですので、このような特殊な問題は避ける傾向にあります。
実際、ヘテロクロマチンのメチル化したヌクレオソームに結合するタンパク質であるHP1が相分離することが2017年に示されてから[5,6]、ヘテロクロマチンというと相分離を連想する人が多いです。
その意味では、私の研究は「物理的」ではない研究だと思います。
しかし、私は、この研究をやりながら、「物理的かそうでないか」よりも、「新しさやオリジナリティーが強いか弱いか」の方が重要だと思いました。
「物理的」を追い求めることによって他の物理の人が独立にほぼ同じことを思いつくことよりも、他の物理の人たちが思いもしないことをする方が創造性が高いですよね。
物理のセンスを持つことは重要ですが、そのセンスは他の物理の人と共通な部分も多いので、頼りすぎると新しさやオリジナリティーが弱くなることに注意が必要です。
ヘテロクロマチンというと相分離を連想してしまう人たちは、高分子の表面吸着との類似性にたどり着くことは難しいでしょう。
そもそも、ヘテロクロマチン形成の一般論があったとして、分裂酵母のヘテロクロマチン形成はその中に入らないのでしょうか。
これまでの物理学では、無駄なものをそぎ落として簡単化することで一般論を構築するアプローチがしばしば取られてきました。
この従来アプローチが生物ではうまくないのではないかと気づき始めたのは、この研究からだったと思います。
新しいサイエンスを作るうえで、常識を疑わなければならない場面は多々あります。
しかし、多くの常識は刷り込まれていて、自分がそのことを常識だと思っていることすら認識していません。
新しいサイエンスを作っていく立場になってから、アインシュタインの言った”Common sense is the collection of prejudices acquired by age eighteen.”(常識とは、18歳までに刷り込まれた偏見のあつまりだ)という意味がよくわかるようになりました。
現在では、学会や研究会など、同じ分野の人たちが情報共有する場が非常に整備されているため、分野の人の間の共通の考えができて、刷り込まれていることもたくさんあるでしょう。
もっと厄介なのは、学生の間に指導教官に刷り込まれることと、学部の講義で刷り込まれることかもしれません。
これらを克服するのは困難を究めます。
異分野の人と研究することは、自分を客観的に見つめなおし、常識と思っていることを認識するきっかけを与えてくれます。
融合研究とはそういうことだと気づいたのも、この研究からだったと思います。
参考文献
1. T. Asanuma, S. Inagaki, T. Kakutani, H. Aburatani, & Y. Murakami, “Tandemly repeated genes promote RNAi-mediated heterochromatin formation via an antisilencing factor, Epe1, in fission yeast”, Genes Dev., 36, 1145-1159 (2022). doi: 10.1101/gad.350129.122
2. S. Emmerth, H. Schober, D. Gaidatzis, T. Roloff, K. Jacobeit, M. Bühler, “Nuclear retention of fission yeast dicer is a prerequisite for RNAi-mediated heterochromatin assembly”, Dev. Cell, 18, 102-113 (2010). doi: 10.1016/j.devcel.2009.11.011.
3. K. Kawakami, A. Hayashi, J. Nakayama, Y. Murakami, “A novel RNAi protein, Dsh1, assembles RNAi machinery on chromatin to amplify heterochromatic siRNA”, Genes. Dev., 26, 1811-1824 (2012) doi: 10.1101/gad.190272.112
4. T. Yamamoto, T. Asanuma, & Y. Murakami, “Polymeric nature of tandemly repeated genes enhances assembly of constitutive heterochromatin in fission yeast”, Comm. Biol., 6, 796 (2023). doi: 10.1038/s42003-023-05154-w
5. A. R. Strom, A. V. Emelyanov, M. Mir, D. V. Fyodorov, X. Darzacq, G. H. Karpen, “Phase separation drives heterochromatin domain formation”, Nature, 547, 241-245. doi: 10.1038/nature22989.
6. A. G. Larson, D. Elnatan, M. M. Keenen, M. J. Trnka, J. B. Johnston, A. L. Burlingame, D. A. Agard, S. Redding, G. J. Narlikar, “Liquid droplet formation by HP1α suggests a role for phase separation in heterochromatin”, Nature, 547, 236–240. doi: 10.1038/nature22822.